Огромный привет Марату! Пусть и дальше всё будет в минусах
Дождались !Идет набор Дельтников на КИ по Мирклюдексу !
Правила форума
Внимание! Администрация форума не имеет никакого отношения к "группе дельтников" в любых мессенджерах, не собирает личные данные пользователей для "включения в группу". Сообщая свой номер телефона кому-либо, вы действуете на свой страх и риск!
Внимание! Администрация форума не имеет никакого отношения к "группе дельтников" в любых мессенджерах, не собирает личные данные пользователей для "включения в группу". Сообщая свой номер телефона кому-либо, вы действуете на свой страх и риск!
- Костян40
- Бывалый
- Сообщения: 37178
- Зарегистрирован: 20 янв 2017 19:10
- Пол: ♂
- Гепатит: С ушел в минус
- Генотип: 3
- Город: Новосибирск
- Благодарил (а): 4810 раз
- Поблагодарили: 4808 раз
Дождались !Идет набор Дельтников на КИ по Мирклюдексу !
Геп С, ген 3- был
Соф/дак 16 нед.
УВО 442
Соф/дак 16 нед.
УВО 442
- Gudvin
- ✔Добрый админ
- Сообщения: 29037
- Зарегистрирован: 24 фев 2009 23:05
- Пол: ♂
- Гепатит: С ушел в минус
- Фиброз: F2
- Генотип: 1
- Город: Million roses city
- Благодарил (а): 1609 раз
- Поблагодарили: 5628 раз
Дождались !Идет набор Дельтников на КИ по Мирклюдексу !
Ты наверное забыл, что на форуме был чат, который вёл Роман? Для тех кому поболтать.
-
Pacha33
- Бывалый
- Сообщения: 1048
- Зарегистрирован: 26 ноя 2017 21:51
- Пол: ♂
- Гепатит: В
- Фиброз: F0
- Генотип: не определял(а)
- Город: Питер
- Благодарил (а): 105 раз
- Поблагодарили: 238 раз
Дождались !Идет набор Дельтников на КИ по Мирклюдексу !
У нас в России проходят прекрасного и первого в мире препарата.это очень большой успех и радость для наших в первую очередь дельтников.тем более цирозников.я многие на форуме хотят видеть результаты хорошие они или плохие.но пусть они будут прозрачные.если что то пойдёт не так мы и тысячи форумчан поддержат наших дельтников.если результаты прекрасными я буду прыгать до потолка от радости.но говорить это их выбор думаю ты лукавишь.позови всех сюда пожалуйста
Ф-0/ гепВ/АЛТ 40/нагрука 2000 МЕ/
- Sovok-59
- Гуру
- Сообщения: 91403
- Зарегистрирован: 25 ноя 2010 12:11
- Пол: ♂
- Гепатит: С ушел в минус
- Фиброз: F1
- Генотип: 1
- Город: Челябинск
- Благодарил (а): 2146 раз
- Поблагодарили: 9552 раза
Дождались !Идет набор Дельтников на КИ по Мирклюдексу !
После чего Ромыч сам и все вместе повесились с сиськами письками
 Мои журналы
Мои журналы описание 2 терапий
описание 2 терапий- kargyraa
- Бывалый
- Сообщения: 2953
- Зарегистрирован: 21 мар 2017 16:00
- Пол: ♂
- Гепатит: Гепатита нет
- Генотип: не определял(а)
- Город: Город Золотой
- Благодарил (а): 178 раз
- Поблагодарили: 1360 раз
Дождались !Идет набор Дельтников на КИ по Мирклюдексу !
Dads
Так можно оправдать любого афериста, обещающего за миллионы рублей излечение неизлечимых болезней. Ведь он же даёт надежду! Ну а те, кому не нравятся аферы - это злые люди, отнимающие надежду!
Вроде бы на форуме обсуждаются зарегистрированные лекарства с доказанной эффективностью, а не циркониевые браслеты и БАДы.
В конце напомню цитату.
Господа интересующиеся Мирклудексом, убедительно прошу изучать первоисточники и вообще вникать в написанное. А то складывается ощущение, что некоторым неважно, ЧТО пишут, а важнее КТО пишет: так удобнее ярлыки навешивать.
Так можно оправдать любого афериста, обещающего за миллионы рублей излечение неизлечимых болезней. Ведь он же даёт надежду! Ну а те, кому не нравятся аферы - это злые люди, отнимающие надежду!
Вроде бы на форуме обсуждаются зарегистрированные лекарства с доказанной эффективностью, а не циркониевые браслеты и БАДы.
В конце напомню цитату.
Вы внимательно читаете тему? Это не мои утверждения, а Совка. Это Совок утверждает, что ни один человек в группе 48 недель монотерапии булевиртидом 10 мг/сутки не достиг ПЦР РНК ВГД "-", в то время как Видемайер опубликовал на AASLD результаты КИ, свидетельствующие о том, что таковых 40%.Roman_T писал(а):На чём основаны Ваши суждения касательно фальсификации публикаций? Есть какие-то неопровержимые доказательства?
Господа интересующиеся Мирклудексом, убедительно прошу изучать первоисточники и вообще вникать в написанное. А то складывается ощущение, что некоторым неважно, ЧТО пишут, а важнее КТО пишет: так удобнее ярлыки навешивать.
Хуун-хуур-ту. "Каргыраа".
- Sovok-59
- Гуру
- Сообщения: 91403
- Зарегистрирован: 25 ноя 2010 12:11
- Пол: ♂
- Гепатит: С ушел в минус
- Фиброз: F1
- Генотип: 1
- Город: Челябинск
- Благодарил (а): 2146 раз
- Поблагодарили: 9552 раза
Дождались !Идет набор Дельтников на КИ по Мирклюдексу !
Не люблю когда врут, предположу что Богомолов написал эту заказуху, а Хайнер даже не знает что его поставили автором этого шедевра
На следующий год планирую в Кельн, заеду спрошу ..
 Мои журналы
Мои журналы описание 2 терапий
описание 2 терапий- Sovok-59
- Гуру
- Сообщения: 91403
- Зарегистрирован: 25 ноя 2010 12:11
- Пол: ♂
- Гепатит: С ушел в минус
- Фиброз: F1
- Генотип: 1
- Город: Челябинск
- Благодарил (а): 2146 раз
- Поблагодарили: 9552 раза
Дождались !Идет набор Дельтников на КИ по Мирклюдексу !
kargyraa,
Когда заказуха не подтверждается фактами, не лучше посмотреть самому анализы больных, постараться понять как происходит излечение и не лезть со всякими статьями рекламного характера времен 90х голов о пользе гептрала и фосфоглива с эссенциале?
Когда заказуха не подтверждается фактами, не лучше посмотреть самому анализы больных, постараться понять как происходит излечение и не лезть со всякими статьями рекламного характера времен 90х голов о пользе гептрала и фосфоглива с эссенциале?
 Мои журналы
Мои журналы описание 2 терапий
описание 2 терапий- kargyraa
- Бывалый
- Сообщения: 2953
- Зарегистрирован: 21 мар 2017 16:00
- Пол: ♂
- Гепатит: Гепатита нет
- Генотип: не определял(а)
- Город: Город Золотой
- Благодарил (а): 178 раз
- Поблагодарили: 1360 раз
Дождались !Идет набор Дельтников на КИ по Мирклюдексу !
Зато благодаря Вам теперь все будут знать, что опубликованные на нынешней конференции AASLD результаты КИ Мирклудекса - рекламная заказуха сродни КИ гептрала, фосфоглива и эссенциале, а проводят КИ Мирклудекса недобросовестные учёные.
AASLD: Safety and Efficacy of 10mg (high-dose) bulevirtide (Myrcludex B) in combination with PEG-IFNa or TDF in patients with chronic HBV/HDV co-infection: interim results. - (12/05/19)
AASLD 2019 Nov 8-11 Boston
Heiner Wedemeyer,
Katrin Schoneweis, Pavel Bogomolov, Natalia Voronkova, Vladimir Chulanov, Tatyana Stepanova, Lena Allweiss, Maura Dandri, Sandra Ciesek, Ulf Dittmer, Walter E. Haefeli, Alexander Alexandrov, Stephan Urban
http://www.natap.org/2019/AASLD/AASLD_68.htm
Хуун-хуур-ту. "Каргыраа".
- Sovok-59
- Гуру
- Сообщения: 91403
- Зарегистрирован: 25 ноя 2010 12:11
- Пол: ♂
- Гепатит: С ушел в минус
- Фиброз: F1
- Генотип: 1
- Город: Челябинск
- Благодарил (а): 2146 раз
- Поблагодарили: 9552 раза
Дождались !Идет набор Дельтников на КИ по Мирклюдексу !
kargyraa,
Ну, это более реально, нет ответа мирк+тдф, есть ответ мирк+Пег
При чем 2, или, 5 или 10 разлет в пределах стат погрешности около 8%
Предварительно даже было 2 лучше ответ чем 10.
Отрезок получается контроля взят всего 48 недель, хотя терапия идет 72 и более.
И потом не показан рецидив после окончания, а он должен быть существенным
И , как по анализам, добавка мирк приводит к повышению солей желчных кислот
PS поэтому 33% ответов на мирк+тдф это была полная чушь, что меня и возмутило..
Ну, это более реально, нет ответа мирк+тдф, есть ответ мирк+Пег
При чем 2, или, 5 или 10 разлет в пределах стат погрешности около 8%
Предварительно даже было 2 лучше ответ чем 10.
Отрезок получается контроля взят всего 48 недель, хотя терапия идет 72 и более.
И потом не показан рецидив после окончания, а он должен быть существенным
И , как по анализам, добавка мирк приводит к повышению солей желчных кислот
PS поэтому 33% ответов на мирк+тдф это была полная чушь, что меня и возмутило..
 Мои журналы
Мои журналы описание 2 терапий
описание 2 терапий- Sovok-59
- Гуру
- Сообщения: 91403
- Зарегистрирован: 25 ноя 2010 12:11
- Пол: ♂
- Гепатит: С ушел в минус
- Фиброз: F1
- Генотип: 1
- Город: Челябинск
- Благодарил (а): 2146 раз
- Поблагодарили: 9552 раза
Дождались !Идет набор Дельтников на КИ по Мирклюдексу !
И, да, чистый Пег дает несколько более высокий уровень минуса, но он, часто наблюдается после 60-72 недели.
Ну и заход на пеги идет не от хорошей жизни, в основном с целью снижения фиброза.
Ну и заход на пеги идет не от хорошей жизни, в основном с целью снижения фиброза.
 Мои журналы
Мои журналы описание 2 терапий
описание 2 терапий- Sovok-59
- Гуру
- Сообщения: 91403
- Зарегистрирован: 25 ноя 2010 12:11
- Пол: ♂
- Гепатит: С ушел в минус
- Фиброз: F1
- Генотип: 1
- Город: Челябинск
- Благодарил (а): 2146 раз
- Поблагодарили: 9552 раза
Дождались !Идет набор Дельтников на КИ по Мирклюдексу !
22 недели, Алексей, мирк10+пегасис180 падение 4 порядка
 Мои журналы
Мои журналы описание 2 терапий
описание 2 терапий-
Pacha33
- Бывалый
- Сообщения: 1048
- Зарегистрирован: 26 ноя 2017 21:51
- Пол: ♂
- Гепатит: В
- Фиброз: F0
- Генотип: не определял(а)
- Город: Питер
- Благодарил (а): 105 раз
- Поблагодарили: 238 раз
Дождались !Идет набор Дельтников на КИ по Мирклюдексу !
Комбинированные схемы с использованием лонафарниба или булевиртида снижали уровни дельта-вируса гепатита (HDV) у большинства людей с коинфекцией HDV и вирусом гепатита B (HBV), сообщили исследователи на встрече AASLD Liver Meeting в прошлом месяце в Бостоне.
HDV - это небольшой дефектный вирус, который может размножаться только в присутствии HBV. По словам доктора Кристофера Коха из Национального института диабета и болезней органов пищеварения и почек, во всем мире около 20 миллионов человек страдают от ВПЧ.
В течение многих лет или десятилетий хронический гепатит В может привести к прогрессирующему заболеванию печени, включая цирроз и рак печени. Ко-инфекция HBV / HDV связана с более быстрым и тяжелым прогрессированием заболевания, чем один гепатит B, и до 80% коинфицированных людей могут заболеть циррозом в течение 5-10 лет, сказал Кох.
Противовирусные препараты , такие как тенофовир дисопроксилфумарат (TDF или Viread ), тенофовир алафенамид (TAF или Vemlidy ) и энтекавир ( Baraclude ), могут подавлять репликацию HBV в течение неопределенного периода времени, но они редко приводят к излечению. В настоящее время нет утвержденного лечения HDV, хотя исследования показали, что пегилированный интерферон может подавлять репликацию HDV по крайней мере временно.
Lonafarnib
Ко представил результаты исследования фазы II ингибитора пренилирования лонафарниб (торговая марка Сарасар ) в сочетании с пегилированным интерфероном лямбда. Лонафарниб блокирует действие фарнезилтрансферазы, фермента, который модифицирует белки посредством процесса, известного как пренилирование. Это мешает сборке и упаковке новых частиц вируса HDV. Пегилированный интерферон лямбда (ранее изученный, но никогда не одобренный для гепатита С) стимулирует иммунную активность против вирусного гепатита с меньшими побочными эффектами, чем пегилированный интерферон альфа.
Предыдущие исследования показали, что лонафарниб снижал уровни РНК HDV в зависимости от дозы в краткосрочных исследованиях, но более высокие дозы приводили к желудочно-кишечным побочным эффектам. Как сообщалось на Встрече печени 2017 года , введение лонафарниба с ритонавиром позволило большему количеству людей принимать эффективные дозы с приемлемыми побочными эффектами.
В исследовании LIFT-HDV участвовало 26 участников. Большинство (60%) составляли мужчины, а средний возраст составлял 40 лет. В начале исследования средний уровень РНК HDV составлял 4,74 log 10 МЕ / мл, а средний уровень АЛТ - 64 МЕ / мл. У них средний балл фиброза Ишака составил 3, что указывает на умеренное повреждение печени, а средний балл жесткости печени FibroScan составлял 11,8 кПа (18 кПа - это обычное ограничение цирроза у людей с гепатитом В).
Все участники этого открытого исследования получали 50 мг лонафарниба, усиленного 100 мг ритонавира, вводимого перорально два раза в день, наряду с 180 мг пегилированного интерферона лямбда, вводимого подкожной инъекцией один раз в неделю в течение 24 недель.
Среди участников, получавших лечение в течение 24 недель, вирусная нагрузка HDV снизилась в среднем на 3,18 log 10 МЕ / мл, что значительно ниже исходного уровня. Среди 19 человек, которые завершили лечение, у всех, кроме одного (95%), снижение РНК HDV более чем на 2 log 10 МЕ / мл и 10 (53%) достигли неопределяемого уровня. Кох сказал, что более низкая вирусная нагрузка HDV на исходном уровне является предиктором ответа.
Лечение в целом было безопасным, хотя побочные эффекты были обычным явлением. Наиболее частыми побочными эффектами были диарея (100%), тошнота (63%), вздутие живота (63%), гастроэзофагеальный рефлюкс (63%), потеря аппетита (47%) и потеря веса (37%). Тем не менее, эти побочные эффекты обычно были слабыми и уменьшались после четырех недель лечения. Около 20% имели повышенный билирубин, известный побочный эффект интерферона лямбда. Три человека снизили дозы лекарств, а четверо прекратили лечение.
«Эти промежуточные результаты подтверждают необходимость дальнейшего изучения этой терапевтической комбинации при ВПЧ», - заключили исследователи.
В настоящее время проводится фаза III исследования усиленного ритонавиром лонафарниба без или без пегилированного интерферона-альфа 2а ( NCT03719313 ).
Bulevirtide
Профессор Heiner Wedemeyer из Университетской клиники Эссена в Германии представил последние результаты исследования фазы IIb другого комбинированного лечения для людей с коинфекцией HBV / HDV, булевиртидом с пегилированным интерфероном альфа или TDF.
Булевиртид, ранее известный как Myrcludex B, является экспериментальным ингибитором проникновения, который связывается с рецептором HBV, используемым для проникновения в клетки печени, нарушая жизненный цикл HBV и тем самым также предотвращая репликацию HDV.
В основное исследование MYR203 были включены 60 человек, которые были случайным образом назначены для приема 2 мг или 5 мг булевиртида путем подкожной инъекции один раз в день плюс 180 мг пегилированного интерферона альфа, вводимого один раз в неделю, 2 мг булевиртида отдельно или пегилированного интерферона в течение 48 недель.
Как сообщил Ведемейер на Международном конгрессе печени EASL в этом году , у 50% участников двух комбинированных групп была обнаружена РНК HDV на 48-й неделе по сравнению с 13% в двух группах монотерапии. На неделе 72 - через шесть месяцев после завершения лечения - у 40% все еще был обнаруживаемый уровень, а у 40% наблюдалась нормализация ALT. Кроме того, 27% достигли потери поверхностного антигена гепатита В (HBsAg) и 20% испытали сероконверсию антител HBs, что считается функциональным излечением. Никто в монотерапевтических отделениях не испытывал стойкого ответа.
На совещании AASLD Ведемейер представил промежуточные результаты расширенной фазы исследования, в ходе которой оценивали 10 мг суточного булевиртида плюс еженедельный пегилированный интерферон альфа или 5 мг булевиртида два раза в день плюс ежедневный TDF в течение 48 недель.
Эти две группы включали 15 пациентов в каждой, все в России. Примерно три четверти составляли мужчины, а средний возраст составлял примерно 37 лет. Средний уровень РНК HDV на исходном уровне составил 6,26 log 10 МЕ / мл, а средний показатель FibroScan составил почти 11.
В конце лечения 87% из тех, кто принимал 10 мг булевтида в день плюс пегилированный интерферон, имели неопределяемую вирусную нагрузку HDV. Частота ответов в течение 48 недель в группе, получавшей 5 мг дважды в день булевиртида и TDF, составила 40%. Частота нормализации ALT на 48 неделе составила 27% и 40% соответственно.
Тем не менее, только один человек, принимавший 10 мг суточного режима булевиртида и пегилированного интерферона, и никто, принимавший комбинацию TDF, не достигли потери HBsAg, не сумев воспроизвести многообещающую частоту функционального излечения, наблюдаемую в основном исследовании. Результаты 72-недельного наблюдения ожидаются.
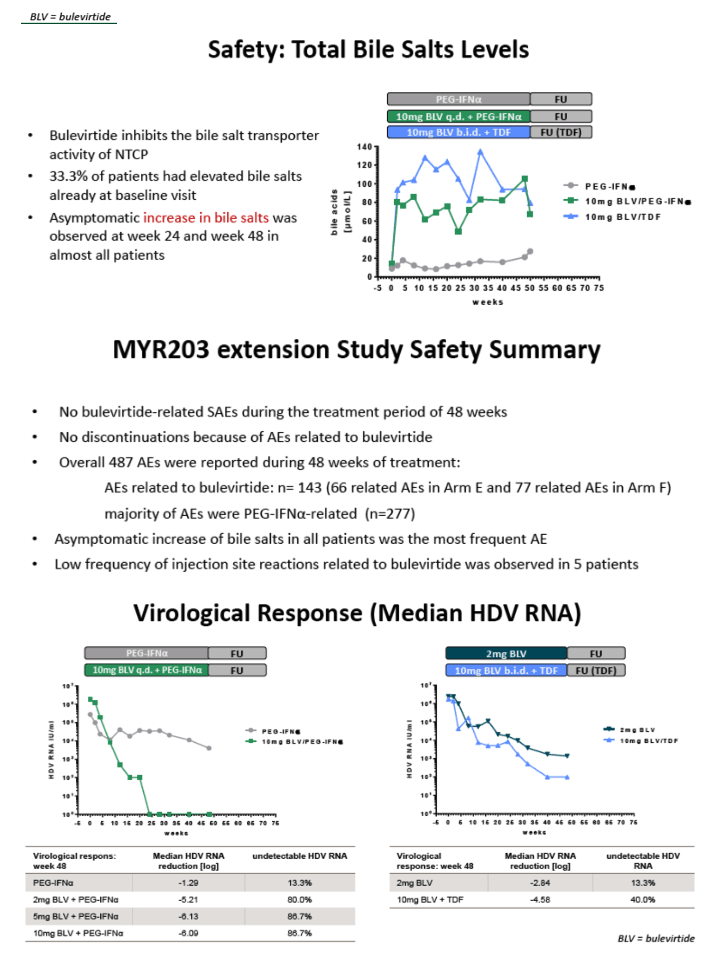
Лечение в целом было безопасным и хорошо переносимым. Большинство неблагоприятных событий были связаны с пегилированным интерфероном. Не сообщалось о серьезных побочных эффектах или прекращении лечения, связанных с булевиртидом. Реакции в месте инъекции были редкостью. Почти все видели бессимптомное увеличение желчных солей, известный побочный эффект булевиртида. В основном исследовании уровни нормализовались вскоре после прекращения терапии.
Ведемейер и его коллеги пришли к выводу, что 10 мг булевиртида в день «является безопасной и многообещающей стратегией для поддерживающей терапии хронического гепатита D», а добавление пегилированного интерферона альфа показывает «сильный синергизм».
В настоящее время проводятся две фазы III испытаний булевиртида, отдельно и в сочетании с пегилированным интерфероном альфа ( NCT03852719 и NCT03852433 ).
HDV - это небольшой дефектный вирус, который может размножаться только в присутствии HBV. По словам доктора Кристофера Коха из Национального института диабета и болезней органов пищеварения и почек, во всем мире около 20 миллионов человек страдают от ВПЧ.
В течение многих лет или десятилетий хронический гепатит В может привести к прогрессирующему заболеванию печени, включая цирроз и рак печени. Ко-инфекция HBV / HDV связана с более быстрым и тяжелым прогрессированием заболевания, чем один гепатит B, и до 80% коинфицированных людей могут заболеть циррозом в течение 5-10 лет, сказал Кох.
Противовирусные препараты , такие как тенофовир дисопроксилфумарат (TDF или Viread ), тенофовир алафенамид (TAF или Vemlidy ) и энтекавир ( Baraclude ), могут подавлять репликацию HBV в течение неопределенного периода времени, но они редко приводят к излечению. В настоящее время нет утвержденного лечения HDV, хотя исследования показали, что пегилированный интерферон может подавлять репликацию HDV по крайней мере временно.
Lonafarnib
Ко представил результаты исследования фазы II ингибитора пренилирования лонафарниб (торговая марка Сарасар ) в сочетании с пегилированным интерфероном лямбда. Лонафарниб блокирует действие фарнезилтрансферазы, фермента, который модифицирует белки посредством процесса, известного как пренилирование. Это мешает сборке и упаковке новых частиц вируса HDV. Пегилированный интерферон лямбда (ранее изученный, но никогда не одобренный для гепатита С) стимулирует иммунную активность против вирусного гепатита с меньшими побочными эффектами, чем пегилированный интерферон альфа.
Предыдущие исследования показали, что лонафарниб снижал уровни РНК HDV в зависимости от дозы в краткосрочных исследованиях, но более высокие дозы приводили к желудочно-кишечным побочным эффектам. Как сообщалось на Встрече печени 2017 года , введение лонафарниба с ритонавиром позволило большему количеству людей принимать эффективные дозы с приемлемыми побочными эффектами.
В исследовании LIFT-HDV участвовало 26 участников. Большинство (60%) составляли мужчины, а средний возраст составлял 40 лет. В начале исследования средний уровень РНК HDV составлял 4,74 log 10 МЕ / мл, а средний уровень АЛТ - 64 МЕ / мл. У них средний балл фиброза Ишака составил 3, что указывает на умеренное повреждение печени, а средний балл жесткости печени FibroScan составлял 11,8 кПа (18 кПа - это обычное ограничение цирроза у людей с гепатитом В).
Все участники этого открытого исследования получали 50 мг лонафарниба, усиленного 100 мг ритонавира, вводимого перорально два раза в день, наряду с 180 мг пегилированного интерферона лямбда, вводимого подкожной инъекцией один раз в неделю в течение 24 недель.
Среди участников, получавших лечение в течение 24 недель, вирусная нагрузка HDV снизилась в среднем на 3,18 log 10 МЕ / мл, что значительно ниже исходного уровня. Среди 19 человек, которые завершили лечение, у всех, кроме одного (95%), снижение РНК HDV более чем на 2 log 10 МЕ / мл и 10 (53%) достигли неопределяемого уровня. Кох сказал, что более низкая вирусная нагрузка HDV на исходном уровне является предиктором ответа.
Лечение в целом было безопасным, хотя побочные эффекты были обычным явлением. Наиболее частыми побочными эффектами были диарея (100%), тошнота (63%), вздутие живота (63%), гастроэзофагеальный рефлюкс (63%), потеря аппетита (47%) и потеря веса (37%). Тем не менее, эти побочные эффекты обычно были слабыми и уменьшались после четырех недель лечения. Около 20% имели повышенный билирубин, известный побочный эффект интерферона лямбда. Три человека снизили дозы лекарств, а четверо прекратили лечение.
«Эти промежуточные результаты подтверждают необходимость дальнейшего изучения этой терапевтической комбинации при ВПЧ», - заключили исследователи.
В настоящее время проводится фаза III исследования усиленного ритонавиром лонафарниба без или без пегилированного интерферона-альфа 2а ( NCT03719313 ).
Bulevirtide
Профессор Heiner Wedemeyer из Университетской клиники Эссена в Германии представил последние результаты исследования фазы IIb другого комбинированного лечения для людей с коинфекцией HBV / HDV, булевиртидом с пегилированным интерфероном альфа или TDF.
Булевиртид, ранее известный как Myrcludex B, является экспериментальным ингибитором проникновения, который связывается с рецептором HBV, используемым для проникновения в клетки печени, нарушая жизненный цикл HBV и тем самым также предотвращая репликацию HDV.
В основное исследование MYR203 были включены 60 человек, которые были случайным образом назначены для приема 2 мг или 5 мг булевиртида путем подкожной инъекции один раз в день плюс 180 мг пегилированного интерферона альфа, вводимого один раз в неделю, 2 мг булевиртида отдельно или пегилированного интерферона в течение 48 недель.
Как сообщил Ведемейер на Международном конгрессе печени EASL в этом году , у 50% участников двух комбинированных групп была обнаружена РНК HDV на 48-й неделе по сравнению с 13% в двух группах монотерапии. На неделе 72 - через шесть месяцев после завершения лечения - у 40% все еще был обнаруживаемый уровень, а у 40% наблюдалась нормализация ALT. Кроме того, 27% достигли потери поверхностного антигена гепатита В (HBsAg) и 20% испытали сероконверсию антител HBs, что считается функциональным излечением. Никто в монотерапевтических отделениях не испытывал стойкого ответа.
На совещании AASLD Ведемейер представил промежуточные результаты расширенной фазы исследования, в ходе которой оценивали 10 мг суточного булевиртида плюс еженедельный пегилированный интерферон альфа или 5 мг булевиртида два раза в день плюс ежедневный TDF в течение 48 недель.
Эти две группы включали 15 пациентов в каждой, все в России. Примерно три четверти составляли мужчины, а средний возраст составлял примерно 37 лет. Средний уровень РНК HDV на исходном уровне составил 6,26 log 10 МЕ / мл, а средний показатель FibroScan составил почти 11.
В конце лечения 87% из тех, кто принимал 10 мг булевтида в день плюс пегилированный интерферон, имели неопределяемую вирусную нагрузку HDV. Частота ответов в течение 48 недель в группе, получавшей 5 мг дважды в день булевиртида и TDF, составила 40%. Частота нормализации ALT на 48 неделе составила 27% и 40% соответственно.
Тем не менее, только один человек, принимавший 10 мг суточного режима булевиртида и пегилированного интерферона, и никто, принимавший комбинацию TDF, не достигли потери HBsAg, не сумев воспроизвести многообещающую частоту функционального излечения, наблюдаемую в основном исследовании. Результаты 72-недельного наблюдения ожидаются.
Лечение в целом было безопасным и хорошо переносимым. Большинство неблагоприятных событий были связаны с пегилированным интерфероном. Не сообщалось о серьезных побочных эффектах или прекращении лечения, связанных с булевиртидом. Реакции в месте инъекции были редкостью. Почти все видели бессимптомное увеличение желчных солей, известный побочный эффект булевиртида. В основном исследовании уровни нормализовались вскоре после прекращения терапии.
Ведемейер и его коллеги пришли к выводу, что 10 мг булевиртида в день «является безопасной и многообещающей стратегией для поддерживающей терапии хронического гепатита D», а добавление пегилированного интерферона альфа показывает «сильный синергизм».
В настоящее время проводятся две фазы III испытаний булевиртида, отдельно и в сочетании с пегилированным интерфероном альфа ( NCT03852719 и NCT03852433 ).
Ф-0/ гепВ/АЛТ 40/нагрука 2000 МЕ/
-
katsavchik
- Новичок
- Сообщения: 12
- Зарегистрирован: 20 дек 2018 17:21
- Пол: ♀
- Гепатит: В+D
- Фиброз: F4
- Генотип: не определял(а)
- Город: Ashdod
Дождались !Идет набор Дельтников на КИ по Мирклюдексу !
Привет всем! Решил написать в Минздрав России, через форму обращения. В ответе на обращение написали, что препарат по которому я обращался, не зарегистрирован. Имеется ввиду Мирклудекс. Так я и не понял, зарегистрирован или нет…


- Gudvin
- ✔Добрый админ
- Сообщения: 29037
- Зарегистрирован: 24 фев 2009 23:05
- Пол: ♂
- Гепатит: С ушел в минус
- Фиброз: F2
- Генотип: 1
- Город: Million roses city
- Благодарил (а): 1609 раз
- Поблагодарили: 5628 раз
Дождались !Идет набор Дельтников на КИ по Мирклюдексу !
Обычная отписка, которая доказывает некомпетентность чиновников. Укажите в следующем письме регистрационный номер ЛП-005945 и пообещайте пожаловаться на несоответствие чиновника занимаемой должности.
-
katsavchik
- Новичок
- Сообщения: 12
- Зарегистрирован: 20 дек 2018 17:21
- Пол: ♀
- Гепатит: В+D
- Фиброз: F4
- Генотип: не определял(а)
- Город: Ashdod
Дождались !Идет набор Дельтников на КИ по Мирклюдексу !
Если не ошибаюсь, то писал и даже ссылку на документ указал. Но я уже снова написал и подробно указал на несоответствие ответа с реальными данными. Жаль, что форма обращения не позволяет сохранять содержание самого обращения. В ответе Минздрава не содержится название препарата, по которому было обращение, странно.

