Статья о наблюдении (
за пределами КИ) за 3 пациентами с компенсированным циррозом, получавшими монотерапию мирклюдекса в максимальной дозировке (10 мг).
Я так понимаю дельту излечить не особо надеются, но планируют эффективно подавлять как нюками при бэшке.
КИ в 3 фазе: хотят проводить монотерапию мирком в течении 3х лет.
https://www.ncbi.nlm.nih.gov/pubmed/31302176
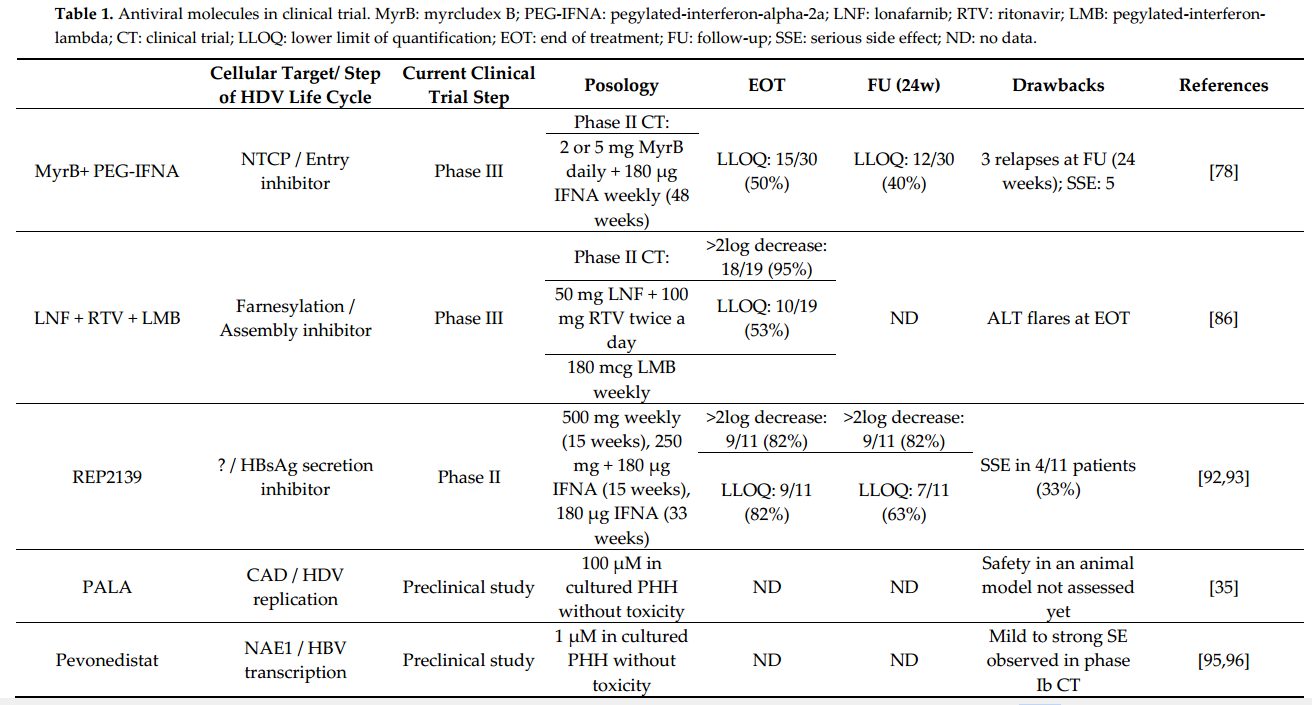
Превосходная безопасность и эффективность монотерапии высокими дозами мирклюкс-b, назначаемой в течение 48 недель при компенсированном циррозе печени, связанном с HDV: история болезни трех пациентов
Было показано, что кратковременное введение ингибитора проникновения Mycludex-B (MyrB) является безопасным и эффективным в исследованиях фазы II у пациентов с коинфекцией HBV / HDV. Тем не менее, его эффективность и безопасность при длительном лечении и лечении высокими дозами при компенсированном циррозе в реальных условиях неизвестны.
Здесь мы описываем первых трех европейских пациентов с компенсированным циррозом печени, вызванным HDV, которые получали терапию MyrB 10 мг/день в течение 48 недель в качестве поддерживающей терапии.
Функциональные тесты печени, желчные кислоты и вирусологические маркеры контролировались каждые 4 недели.
В двух случаях оценивали также HDV/HBV-специфическое количество Т-клеток (до 48 и 36 недель) и уровни РНК HBV.
Во время лечения MyrB уровни РНК HDV постепенно снижались с 4,4 и 5,6 log МЕ/мл до необнаруживаемости в первых двух случаях
и с 6,8 log коп/мл до 500 коп/мл для другого пациента.
АЛТ нормализовалось через 20, 12 и 28 недель соответственно.
Значительное улучшение характеристик портальной гипертензии, тестов функции печени и уровня АФП было зафиксировано в двух случаях.
У пациента мужского пола с гистологическими и клиническими признаками аутоиммунного гепатита, IgG и иммуноглобулины быстро нормализовались.
Не было выявлено значительных изменений уровней HBsAg и циркулирующих HDV / HBV-специфических Т-клеток;
уровни ДНК HBV и РНК HBV оставались необнаружимыми в течение всего периода исследования.
MyrB хорошо переносился; пациенты оставались полностью бессимптомными, несмотря на значительное увеличение желчных кислот.
В заключение, этот отчет показывает превосходную безопасность и эффективность 48-недельного курса 10 мг/день MyrB
в сочетании с TDF для лечения HDV-пациентов c компенсированным циррозом.
Введение
Вирус гепатита (HDV) - это дефектный РНК-вирус, обнаруженный в 1977 году, для которого требуется присутствие поверхностного антигена HBV (HBsAg), чтобы обернуть его вирусный рибонуклеопротеиновый комплекс, чтобы стать инфекционным.
Приблизительно 15–20 миллионов пациентов во всем мире имеют свидетельства хронического гепатита, вызванного HDV, который обычно показывает более быстрое прогрессирование до цирроза (4% в год) и вызывает больше осложнений, чем пациенты с моноинфекцией HBV.
На сегодняшний день единственная доступная терапия, пегилированный интерферон (Peg-IFN), который обладает значительными побочными эффектами и ингибирует репликацию HDV только у меньшинства пациентов [1].
Тем не менее, терапевтический ландшафт терапии HDV быстро меняется, так как перспективные новые соединения, такие как монотерапия или в сочетании с Peg-IFN, в настоящее время исследуются в фазах I и II клинических испытаний [2].
Среди этих новых стратегий интересные свойства имеет ингибитор проникновения пептида MyrB, нацеленный на обычно используемый HBV и HDV рецептор (транспортировочный полипептид натрия-таурохолат, NTCP).
В исследованиях фазы II у пациентов, которые получали монотерапию MyrB в дозе 2 или 5 мг/день в течение до 48 недель,
наблюдалось значительное снижение уровней РНК HDV в сыворотке в сочетании с нормализацией ALT [3,4].
При комбинировании с Peg-IFN в течение 48 недель показатели вирусологического подавления дополнительно улучшались
(50% против 13% в группе монотерапии Peg-IFN), и потеря HBsAg происходила у 13% пациентов в комбинированных группах (по сравнению с 0/15 пациенты) в группе монотерапии Пег-ИФН) [5].
MyrB был безопасным и хорошо переносимым, несмотря на значительное увеличение общего количества желчных кислот [6],
что коррелирует с ингибированием основного переносчика конъюгированной желчной соли NTCP.
Следовательно, введение MyrB может предоставить новую терапевтическую возможность для пациентов с HDV, особенно для тех, кто срочно нуждается в лечении, таких как пациентов с циррозом или пациентов, которым противопоказано применение IFN из-за тяжести заболевания или предшествующего отсутствия ответа на терапию [7 ].
Примечательно, что пока не было никаких данных о терапии с применением высокими доз MyrB в течение более 24 недель.
Таким образом, это первый отчет, нацеленный на описание безопасности и эффективности MyrB 10 мг/день, вводимого в течение 48 недель
у первых трех европейских пациентов с компенсированным циррозом печени,
получавших лечение вне клинических испытаний.
После одобрения Этическим комитетом (EC) использования MyrB в качестве поддерживающей <compassionate = сострадательной> терапии
для двух итальянских пациентов и письменного информированного согласия для австрийского пациента,
MyrB был добавлен к продолжающейся терапии тенофовир-дисопроксилфумаратом (TDF).
MyrB вводился самостоятельно в виде двух подкожных инъекций каждые 24 часа (2 флакона по 5 мг каждый).
Функциональные пробы печени, общее количество желчных кислот и вирусологические маркеры HDV и HBV контролировали каждые 4 недели.
///
Аутоантитела и иммуноглобулины оценивали каждые шесть месяцев, жесткость печени по Fibroscan® каждые 3-6 месяцев,
ультразвуковое исследование брюшной полости каждые 6 месяцев.
В двух случаях были проведены дополнительные анализы.
РНК HBV тестировали каждые 12 недель лечения с использованием специальной методики ПЦР в реальном времени:
для достижения высокой чувствительности для экстракции нуклеиновой кислоты использовали 200 мкл сыворотки (нижний предел детекции 160 копий/мл).
В мононуклеарных клетках периферической крови (PBMC), собранных и криоконсервированных каждые 4 недели, количество и функцию HDV/HBV-специфических Т-клеток анализировали прямыми методами IFN-γ ELISPOT ex-vivo с использованием перекрывающихся пептидов (15 мер/перекрытие 10AA), охватывает как протеомы HBV, так и HDV.
Положительность единиц формирования пятна (SFU) определяется, когда значения были выше порога (который в 3 раза выше лунок отрицательного контроля).
Пациенты предоставили письменное информированное согласие на хранение и анализ дополнительной пробы сыворотки.
Пациент № 1
69-летняя женщина, европейского происхождения {сaucasian=белая}, HBeAg-отрицательная пациентка с компенсированным циррозом печени, связанным с HDV (A5 по шкале Чайлд-Пью ), осложненным портальной гипертензией (спленомегалия и тромбоцитопения), была рекомендована для лечения MyrB в январе 2018 года, так как терапия интерфероном была противопоказана из-за возраста, количества тромбоцитов и предыдущего отсутствия ответа.
У нее был генотип D для HBV и генотип 1 для HDV.
В 2011 году она лечилась альфа-ПЭГ-ИФН 135 мкг/неделю в течение 18 месяцев с нормализацией уровней АЛТ и неопределяемой РНК HDV во время терапии, но с вирусологическим и биохимическим рецидивом после отмены интерферона.
Для контроля репликации вируса гепатита В в 2012 году был начат прием TDF 245 мг/48 часов.
С января 2014 года уровни ALT оставались неизменно высокими (100-150 ед/л), при этом виремия HDV постоянно обнаруживалась.
У нее был сахарный диабет, она получала диетическую терапию (индекс массы тела, ИМТ, 23,4 кг/м2), остеопения бедра и поясницы,
а также легкая артериальную гипертензию.
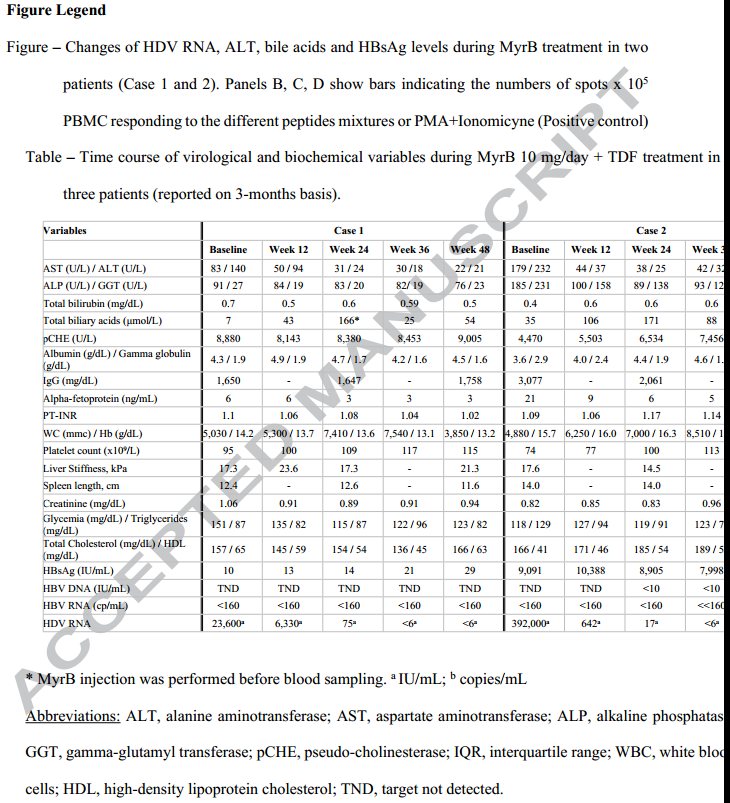
В таблице приведены наиболее важные базовые характеристики.
После введения MyrB 10 мг/день РНК HDV постепенно снижалась с 4,4 log МЕ/мл до неопределяемой через 36 недель,
в то время как уровни ALT нормализовались через 20 недель (рисунок).
Вирусологические и биохимические реакции сохранялись во время терапии.
Уровень АФП в сыворотке крови снизился с 6 до 3 нг/мл, улучшились тесты функции печени, а также количество тромбоцитов (таблица).
Уровни HBsAg и жесткость печени немного увеличились (с 10 до 29 МЕ/мл; с 17,3 до 21,3 кПа).
Инъекции MyrB переносились хорошо, кожных реакций или проблем, связанных с приемом лекарств, не было.
Значительное увеличение общего количества желчной кислоты оставалось бессимптомным (рисунок).
Несмотря на падение значений РНК HDV, мы не обнаружили какого-либо повышенного HDV-специфического ответа Т-клеток,
в то время как только одна определяемая флуктуация ответа Т-клеток на белок HBV (полимеразу) была на 20 неделе (рисунок, панель B).
Уровни РНК HBV в сыворотке были ниже предела детекции в начале и во все моменты времени во время лечения MyrB (рисунок)
Пациент № 2
51-летний белый мужчина, HBeAg-отрицательный пациент с компенсированным циррозом, вызванным HDV (A5 по шкале Чайлд-Пью),
осложненным спленомегалией, тромбоцитопенией и небольшими варикозом вен пищевода,
был выбран для терапии MyrB в мае 2018 года.
У него был генотип D для HBV и генотип 1 для HDV.
Коинфекция HDV/HBV была известна с июня 2010 года, когда пациенту была сделана биопсия печени с показателем гепатита,
ассоциированного с HDV, с оценкой от средней до тяжелой степени (9 класс, стадия 6, по шкале Ишака)
со значительным компонентом плазматической клетки.
С 2012 года уровни АЛТ оставались повышенными (150-200 Ед/л) с постоянно обнаруживаемой виремией HDV.
У него был диабет, он находился на диетотерапии (ИМТ 22,7 кг/м2), и он получил TDF 245/24 ч (с 2012 года) и добавку витамина D.
Интерфероновая терапия была противопоказана из-за тяжести заболевания, низкого количества тромбоцитов и аутоиммунных признаков при гистологии.
Наиболее важные исходные демографические, клинические и вирусологические особенности приведены в табл.
Во время терапии MyrB 10 мг/день РНК HDV снизилась с 5,6 log МЕ / мл и стала необнаружимой через 28 недель,
а уровни АЛТ нормализовались всего за 8 недель (рисунок).
Эти ответы были сохранены до 48 недели, во время последнего визита, зарегистрированного здесь.
Уровни AST, ALP и AFP нормализовались параллельно (AFP от 21 до 5 нг/мл), тогда как уровни GGT значительно улучшились.
Функциональные пробы печени (альбумин от 3,6 до 4,4 г/дл, pCHE от 4470 до 6648 ед/л),
а также функции портальной гипертензии (количество тромбоцитов от 74 до 111x10^9 /л),
жесткость печени (от 17,6 до 10,1 кПа) и HBsAg уровни (от 9 091 до 7 499 МЕ / мл) улучшились.
Следует отметить также иммунологические маркеры, такие как IgG и гаммаглобулин уровни значительно улучшились во время терапии (таблица).
MyrB был хорошо переносим; о симптомах не сообщалось, несмотря на увеличение желчных кислот, которое сохранялось на протяжении всей терапии (рисунок).
Несмотря на глубокое снижение РНК HDV, восстановления реакции HDV или HBV-специфических Т-клеток не наблюдалось.
Они оставались ниже уровня позитивности (в 3 раза выше фонового уровня) на протяжении всего исследования (рис., Панели B и C).
Уровни РНК HBV в сыворотке снова были ниже предела детекции в начале и во все моменты времени во время лечения (таблица)
Пациент № 3
58-летняя женщина, уроженка Узбекистана, наблюдалась с 2012 года как инфецированная HBV + HDV .
Как положительная HBsAg она была известна с 1988 года.
Биопсия печени никогда не проводилась, но на основании результатов ультразвукового исследования было предложен компенсированный цирроз печени.
Она была HBeAg-отрицательной, ДНК HBV была 4850 МЕ / мл, РНК HDV 6,2 log коп/мл.
Она начала принимать TDF 245 мг/день, а через 3 месяца она получила Peg-IFN альфа 180 мкг/неделя, который, однако, был прекращен
из-за повышения уровня ALT и значительного снижения количества тромбоцитов до 5x10^9 /л из-за аутоиммунной тромбоцитопении
с детектируемыми антителами против тромбоцитов.
Она получала высокие дозы лечения преднизолоном, постепенно снижающиеся. Следующие три года она не получала дополнительной терапии,
ее уровень тромбоцитов был стабильным в пределах нормы, но ее трансаминазы оставались между 200 и 450 Ед/л из-за HDV.
Поскольку терапия интерфероном была противопоказана из-за аутоиммунной тромбоцитопении в анамнезе, MyrB 10 мг/день был начат в апреле 2018 года.
Наиболее важные исходные демографические, клинические и вирусологические особенности приведены в табл.
РНК HDV прогрессивно снижалась в течение MyrB с 6,8 log коп/ml до 500 коп/ml к 48 неделе, снижение на 4,1 log коп/мл,
ALT нормализовалось к 28 неделе, в то время как уровни HBsAg оставались неизменными.
Несмотря на значительное увеличение желчных кислот, о симптомах не сообщалось (таблица).
Обсуждение
Этот отчет продемонстрировал эффективность и безопасность 48-недельного введения MyrB 10 мг/день у трех пациентов с компенсированным циррозом печени, связанным с HDV. Насколько нам известно, это первое описание подобной терапии.
Пациенты показали быструю нормализацию трансаминаз, и глубокое снижение уровней РНК сыворотки HDV с клинически значимым улучшением функции печени в контексте превосходного профиля безопасности.
Ответы сохранялись в течение всего периода терапии.
Эти три случая помогают получить дополнительные знания о профиле безопасности MyrB в «полевых условиях»,
так как нет опубликованных исследований, описывающих безопасность и переносимость MyrB 10 мг в течении 48 недель.
Лечение хорошо переносилось всеми тремя пациентами, без серьезных нежелательных явлений.
Как и следовало ожидать, учитывая режим действия препарата и в соответствии с фазой II КИ[6], желчные кислоты значительно увеличивались на протяжении всего периода исследования, но пациенты оставались полностью бессимптомными.
Интересно, когда анализы крови делались после введения MyrB, а не до того, как было рекомендовано, уровни желчных кислот еще более увеличивались, превышая 100 мкмоль / л, но опять же пациенты оставались полностью бессимптомными.
Второй важной новой информацией является эффективность этого подхода, так как ни одно исследование пока не сообщало
о противовирусном и биохимическом ответе на 10 мг/день MyrB, вводимого в течение 48 недель.
Все три пациента, получавшие монотерапию MyrB, не только достигли недавно рекомендованной конечной точки в снижения РНК HDV более, чем на 2 log и нормализации АЛТ [8], но также испытали глубокое подавление репликации вируса со снижением РНК HDV на 4,0-5,0 log .
Следует отметить, что виремия стала необнаружимой у двух пациентов.
Эти результаты соответствуют опубликованным результатам исследований MYR, которые показали прогрессивное дозозависимое снижение РНК HDV.
Неопределимость HDV-РНК была достигнута у 3,3–6,2% пациентов, получавших различные дозы в течение 24 недель в исследовании MYR 202
(личное сообщение от MYR GmbH), и у 2 из 15 (13%) пациентов, получавших 2 мг/день в течение 48 недель [5].
Следует отметить, что в клинических испытаниях MYR 202 в течение 24 недель лечения было показано, что 10 мг вызывают более резкое снижение РНК HDV, чем 2 мг.
Кинетика биохимических и вирусологических ответов у наших пациентов продемонстрировала, что ответ ALT был быстрее, чем ответ РНК HDV,
что согласуется с предыдущими исследованиями фазы II.
Наконец, что не менее важно, вирусологические и биохимические реакции сохранялись в течение долгого времени без каких-либо доказательств вирусологического или биохимического прорыва, а также увеличения ДНК HBV.
По сравнению с монотерапией ИФН, которая обладает ограниченной эффективностью и значительными побочными эффектами,
этот отчет подтверждает возможность стратегии против HDV, основанной на длительном применении монотерапии MyrB, направленной на подавление вирусной нагрузки и, возможно, внутрипеченочной репликации вируса до необнаружимых уровней.
У пациентов с противопоказаниями или не отвечающими на IFN монотерапия MyrB может представлять собой жизнеспособный терапевтический вариант.
Тем не менее, поскольку нет исследований, оценивающих эффективность и безопасность MyrB в случае
декомпенсированного цирроза,
использование MyrB в этом случае потребует специальных клинических испытаний.
Исследование также содержит важные клинические данные.
Биохимические и вирусологические реакции предшествовали улучшению показателей функции печени, уровня АФП и количества тромбоцитов.
Эти данные имеют клиническую значимость, учитывая хорошо известную агрессивность дельта-гепатита и относительную короткую продолжительность терапии у этих пациентов.
Кроме того, в случае 2, который имел гистологические и клинические признаки аутоиммунного гепатита, вторичного к инфекции HDV,
(не редкое состояние у пациентов, инфицированных HDV),
IgG и гамма-глобулины, нормализовались параллельно с уменьшением РНК HDV.
Это может иметь клиническое значение у пациентов с HDV-инфекцией и аутоиммунными признаками, что в настоящее время является противопоказанием к введению ИФН.
Наконец, два случая были также проверены на наличие дополнительных маркеров, направленных на изучение паттерна активации Т-клеток.
Несмотря на вирусологический ответ, мы не обнаружили каких-либо признаков восстановления специфического для HDV и HBV Т-клеточного ответа у этих двух пациентов, получавших MyrB. Однако анализ влияния терапии MyrB на восстановление HDV и HBV-специфических Т-клеток требует более масштабных исследований,
и пациенты младшего возраста, которые часто характеризуются более консервативным антивирусным репертуаром Т-клеток.
Кроме того, нельзя исключать возможность того, что ингибирование HDV повлияет на глобальный профиль иммунитета,
и необходим более глобальный анализ других компонентов иммунной системы (B, NK и миелоидных клеток).
Уровни РНК HBV были ниже предела обнаружения до и во время лечения MyrB, что, вероятно, отражает низкую транскрипцию РНК HBV из
ковалентно закрытой кольцевой ДНК (cccDNA). Это может быть связано с отрицательным статусом HBeAg, а также с предшествующим длительным периодом лечения TDF (> 6 лет) у обоих пациентов или ограниченной чувствительностью метода. Коинфекция HDV, возможно, также сыграла значительную роль.
Предполагая, что активность cccDNA была низкой, обнаруженный HBsAg, вероятно, был преимущественно получен из интегрированного генома HBV.
Вопрос о том, может ли 48-недельный курс 10 мг / день MyrB привести к устойчивому, то есть в отсутствии лечения, вирусологическому и биохимическому ответу, является серьезным вопросом. Тем не менее, в настоящее время это неизвестно, так как ни одно исследование пока не оценило этот режим, и все наши пациенты планируют продолжать MyrB после 48 недели.
Фактически, исследование MYR 202 ясно продемонстрировало, что 24-недельный курс MyrB не вызывает долгосрочных ответов после лечения, хотя приблизительно 10% пациентов поддерживали нормальные уровни ALT и имели РНК HDV <2 log IU / мл через 24 недели после прекращение лечения.
Подобные результаты недавно были опубликованы на EASL 2019: только 2 из 15 (13%) пациентов, получавших монотерапию MyrB 2 мг в течение 48 недель, поддерживали комбинированный ответ на РНК HDV и ALT через 24 недели после лечения (H.Wedemeyer и др. EASL 2019 G13 ; J Hepatol 2019; 70 (S): e81).
Как показывают недавние модели in vitro, вполне вероятно, что лечение должно быть продлено гораздо дольше 48 недель.
Действительно, монотерапия MyrB будет проводиться в течение 3 лет в фазе 3 исследования.
Будут ли долгосрочные ответы вне лечения без потери HBsAg, будут изучены в последующих исследованиях.
В заключение, это первое сообщение о наблюдении за терапией MyrB в дозе 10 мг/день в течение 48 недель у трех пациентов с компенсированным циррозом печени, связанным с HDV.
Отличный вирусологический и биохимические реакции, индуцированные и поддерживаемые длительным введением монотерапии MyrB в сочетании с благоприятным профилем безопасности, могут представлять интересный терапевтический подход для трудно поддающегося лечению и агрессивного заболевания, такого как дельта-гепатит. Долгосрочные исследования в большее количество пациентов требуется для подтверждения этих предварительных результатов.
Статья в препринтном формате, поэтому таблица к сожалению срезана




 Подробнее
Подробнее